 2.1 钠及其化合物 教案
2.1 钠及其化合物 教案
《2.1 钠及其化合物 教案》由会员分享,可在线阅读,更多相关《2.1 钠及其化合物 教案(5页珍藏版)》请在七七文库上搜索。
1、2.1 钠及其化合物钠及其化合物 一、教学目标 1了解钠的物理性质,了解钠与氧气、钠与水的反应与现象 2结合真实情境中的应用实例或通过实验探究,了解钠及其重要化合物的主要性质 3了解 Na2CO3和 NaHCO3的共性和差异性 二、教学重难点 1. 教学重点 钠的氧化和钠与水的反应;碳酸钠和碳酸氢钠的性质比较 2. 教学难点 钠与水的反应;碳酸钠和碳酸氢钠的性质比较 三、教学过程 教学环节 教学内容 设计意图 1.新课导入 同学们,今天我们来认识认识一种新的金属,说到金属,同学们会想起 初中学过的金属的活动性顺序。 在初中我们也学过一些金属, 例如:铝、铁、 铜。这是我们生活中常见的金属。但是
2、今天我们要学习的金属钠是平时生活 中不常见的。下面我们就一起来探究钠的物理化学性质。 联系实际生 活, 情景带入 2.探索新知 【知识回顾】1、金属的物理通性:金属光泽、延展性、导电性、导热性 2、绝大多数金属元素在自然界中以化合物的形式存在 【师】一、钠单质 1. 钠的物理性质 【实验 2-1】切开金属钠前先观察钠的表面,以便与切后进行比较。切割金 属钠在玻璃片上进行。 【学生活动】观察现象:取出的金属钠表面有一灰黄色层,切开后的切口处 露出银白色光泽;切口在空气中露置一会儿,会逐渐变暗;久置表面还会形 成溶液,再变成白色粉末。 【师】实验说明,钠具有金属光泽,质软。放置后,钠表面逐渐变暗生
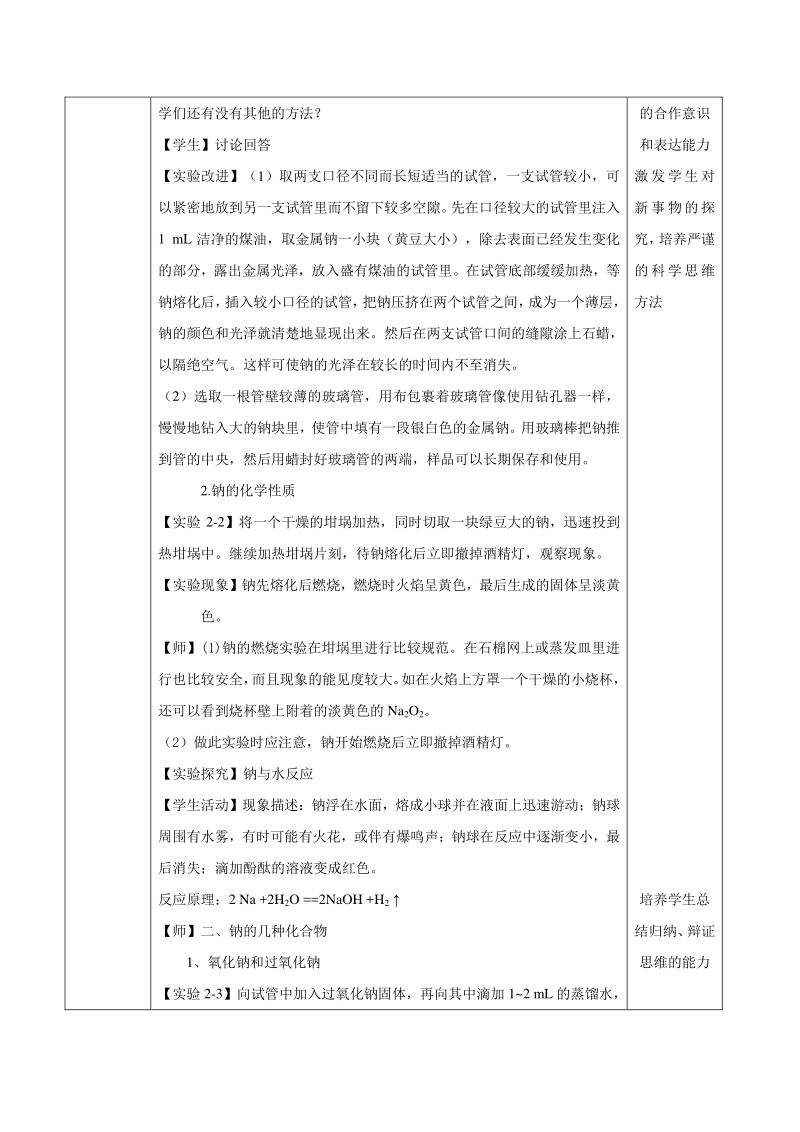
3、成新 物质。 【思考与讨论】提问:考虑到实验的安全性与可操作性,对此实验的探究同 通过探讨交 流培养学生 学们还有没有其他的方法? 【学生】讨论回答 【实验改进】(1)取两支口径不同而长短适当的试管,一支试管较小,可 以紧密地放到另一支试管里而不留下较多空隙。 先在口径较大的试管里注入 1 mL 洁净的煤油,取金属钠一小块(黄豆大小),除去表面已经发生变化 的部分,露出金属光泽,放入盛有煤油的试管里。在试管底部缓缓加热,等 钠熔化后, 插入较小口径的试管, 把钠压挤在两个试管之间, 成为一个薄层, 钠的颜色和光泽就清楚地显现出来。然后在两支试管口间的缝隙涂上石蜡, 以隔绝空气。这样可使钠的光泽
4、在较长的时间内不至消失。 (2)选取一根管壁较薄的玻璃管,用布包裹着玻璃管像使用钻孔器一样, 慢慢地钻入大的钠块里,使管中填有一段银白色的金属钠。用玻璃棒把钠推 到管的中央,然后用蜡封好玻璃管的两端,样品可以长期保存和使用。 2.钠的化学性质 【实验 2-2】将一个干燥的坩埚加热,同时切取一块绿豆大的钠,迅速投到 热坩埚中。继续加热坩埚片刻,待钠熔化后立即撤掉酒精灯,观察现象。 【实验现象】钠先熔化后燃烧,燃烧时火焰呈黄色,最后生成的固体呈淡黄 色。 【师】(1)钠的燃烧实验在坩埚里进行比较规范。在石棉网上或蒸发皿里进 行也比较安全, 而且现象的能见度较大。 如在火焰上方罩一个干燥的小烧杯,
5、还可以看到烧杯壁上附着的淡黄色的 Na2O2。 (2)做此实验时应注意,钠开始燃烧后立即撤掉酒精灯。 【实验探究】钠与水反应 【学生活动】现象描述:钠浮在水面,熔成小球并在液面上迅速游动;钠球 周围有水雾,有时可能有火花,或伴有爆鸣声;钠球在反应中逐渐变小,最 后消失;滴加酚酞的溶液变成红色。 反应原理:2 Na +2H2O =2NaOH +H2 【师】二、钠的几种化合物 1、氧化钠和过氧化钠 【实验 2-3】向试管中加入过氧化钠固体,再向其中滴加 12 mL 的蒸馏水, 的合作意识 和表达能力 激发学生对 新事物的探 究, 培养严谨 的科学思维 方法 培养学生总 结归纳、 辩证 思维的能力


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2.1 钠及其化合物 教案 及其 化合物
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-152965.html