 3.3.1金属晶体 离子晶体ppt课件1
3.3.1金属晶体 离子晶体ppt课件1
《3.3.1金属晶体 离子晶体ppt课件1》由会员分享,可在线阅读,更多相关《3.3.1金属晶体 离子晶体ppt课件1(41页珍藏版)》请在七七文库上搜索。
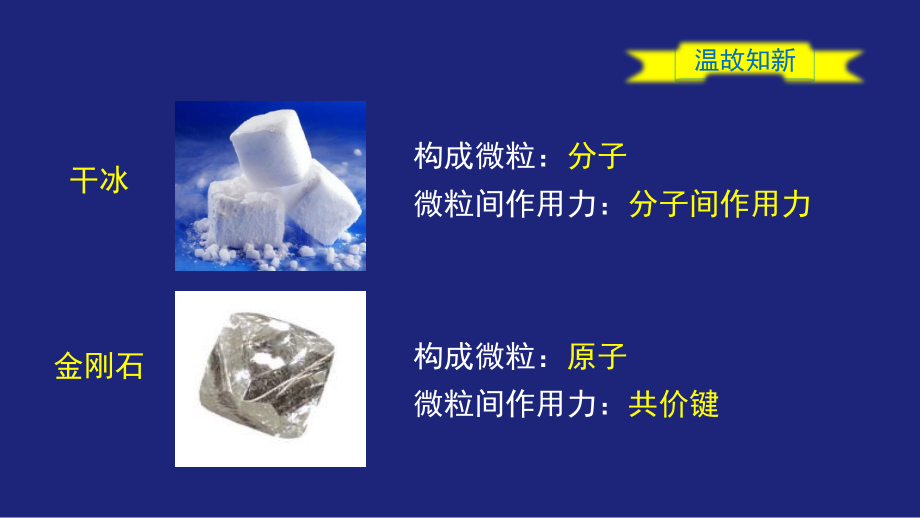
1、第三章 晶体结构与性质 第1课时 金属晶体 离子晶体 第三节 金属晶体与离子晶体 学习目标 1. 能说出金属键、离子键的特征和实质。 2. 能运用金属晶体模型,从微观视角解释金属晶体的 宏观性质。 3. 能以 NaCl、CsCl 为例解释典型离子化合物的某些性质。 构成微粒:分子 微粒间作用力:分子间作用力 干冰 温故知新 金刚石 构成微粒:原子 微粒间作用力:共价键 丰富多彩的金属 新课引入 容易导电、导热、有延展性、有金属光泽等。 回顾思考:金属有哪些物理性质? 为什么金属能够导电、导热、有延展性、有金属光泽? 什么作用力使金属保持固定的形状? 一、金属晶体 1. 构成微粒:金属阳离子和自
2、由电子 2. 微粒间作用:金属键 金属(除汞外)在常温下都是晶体,称其为金属晶体 金属键 金属晶体的电子气理论示意图 价电子脱落 遍布整块晶体的“电子气” 价电子被所有原子共用 金属键 “巨分子” 没有饱和性和方向性 金属键无饱和性和方向性 铜晶体 水果的密堆积 金属晶体可以看作 X 射线衍射实验充分验证了这些事实 等径圆球 在三维空间堆积而成 电子定向移动 通电 导电 电子运动没有固定方向 未通电 导电性 金属的性质- 不同金属导电能力不同,导电性较强的三种金属是 Ag、Cu、Al Ag Cu Al 从一点加热 自由电子与金属原子 高速碰撞 能量被传导 加热点 低温区 高温区 导热性 金属的
3、性质- 自由电子与金属原子 频繁碰撞 加热 金属的电导率下降 延展性 金属的性质- 外力 电子起到润滑剂的作用 各原子层发生相对滑动 光泽性 金属的性质- 金属晶体对辐射具有良好的 反射性能,金属中自由电子可以 吸收波长极广的光,并重新反射 出来。 金属晶体 不透明 且有金属光泽 金属晶体有导电性,能导电的物质都属于金属晶体吗? 问题 1 不一定 常温下金属汞也能导电 NaCl 溶液、熔融态 NaCl 石墨、聚乙炔等也能导电 以上物质都不属于金属晶体 金属导电与电解质导电有什么不同? 自由移动的离子 自由电子 类别 电解质 金属晶体 导电时的状态 导电粒子 导电时发生的变化 化学变化 物理变化
4、 水溶液或 熔融状态下 晶体状态 问题 2 合金的硬度一般比成分金属大,你知道其中的原因吗? 当向金属晶体中掺入不同的金属或非金属原子时, 就像在滚珠之间掺入了细小而坚硬的沙土或碎石一样, 会使这种金属的延展性和硬度发生改变。 问题 3 钠:熔点较低、硬度较小 钨:熔点最高 铬:硬度最大 问题 4 金属键 的强弱 离子半径越小 电荷越多 金属键 越强 熔沸点越高 硬度越大 A A Li Na Mg K Rb Cs 0 A A A A A Al s 区 ns1-2 熔点升高 熔 点 降 低 为什么? 半径依次减小,阳离子电荷数依次增多,金属键强度增强 半径依次增大,阳离子电荷数相同,金属键强度减
5、弱 熔点最低 汞 密度最小 锂 硬度最大 铬 金属的用途 硬度大 密度小 硬铝 重晶石 BaSO4 莹石 CaF2 胆矾 CuSO4 5H2O 明矾 KAl(SO4)2 12H2O 下列晶体构成微粒有什么共同点? 微粒之间存在哪种相同的作用力? 二、离子晶体 由阳离子与阴离子相互作用而形成的晶体,叫离子晶体 1. 构成微粒: 2. 微粒间相互作用: 离子键 阴、阳离子 阴、阳离子间的静电作用 2Na + Cl2 2NaCl + Na+ Cl Na Cl Cl Na+ 3. NaCl 离子晶体及晶胞结构特点 离子键! 静电作用 NaCl 的晶胞 12 + 1 = 4 1 4 数 = 8 + 6


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 3.3
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-197421.html