 2023年广东省中考化学一轮复习考点专题1:物质的性质与应用 第6讲溶液(含答案)
2023年广东省中考化学一轮复习考点专题1:物质的性质与应用 第6讲溶液(含答案)
《2023年广东省中考化学一轮复习考点专题1:物质的性质与应用 第6讲溶液(含答案)》由会员分享,可在线阅读,更多相关《2023年广东省中考化学一轮复习考点专题1:物质的性质与应用 第6讲溶液(含答案)(20页珍藏版)》请在七七文库上搜索。
1、专题1 物质的性质与应用第06讲 溶液考点归纳必考点1 溶液的形成1.溶液的概念:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物。2.特征:(1)均一性:溶液各部分的组成相同;(2)稳定性:外界条件不变时,溶质和溶剂不会分离。3.溶液的组成:溶液由溶质和溶剂组成,其溶液质量为m溶液 = m溶质+ m溶剂。4.溶质溶解时的吸、放热现象溶解放热的物质有NaOH等,溶解吸热的物质有NH4NO3等,热效应不明显的物质有NaCl等。5.乳化现象洗涤剂把油污分散成无数细小的液滴,而不聚集成大的油珠。洗涤剂所起的作用叫乳化作用。6.易错点(1)溶液一定是一种混合物。(2)溶液不一定都是无色的,如硫
2、酸铜溶液是蓝色的。(3)均一稳定的液体不一定是溶液,如水是纯净物。(4)乳化现象是物理变化,汽油溶解油污也是物理变化,纯碱去油污属于化学变化。(5)CaO加入水中也会放热,但它是与水反应生成Ca(OH)2的过程放热,属于化学变化。【考点突破】1.将一定量的下列固体放入适量水中,能形成溶液且温度明显升高的是( )ACaCO3BNaOHCNaClDNH4NO3【答案】B【解析】A、碳酸钙不溶于水,不能形成溶液,故选项错误;B、氢氧化钠溶于水放出大量的热,溶液温度升高,故选项正确;C、氯化钠溶于水温度变化不大,故选项错误;D、硝酸铵溶于水时吸收热量,溶液温度降低,故选项错误。故选:B。2.下列物质加
3、入水中,能形成溶液的是()A沙子B食盐C植物油D面粉【答案】B【解析】A、沙子难溶于水,沙子颗粒悬浮于水中,形成悬浊液,不能形成溶液,A不符合题意;B、食盐的主要成分是氯化钠,氯化钠溶于水,能形成均一、稳定的混合物,能形成溶液,B符合题意;C、植物油不溶于水,以小液滴分散到液体里形成乳浊液,不能形成溶液,C不符合题意;D、面粉难溶于水,面粉颗粒悬浮在水中,形成悬浊液,不能形成溶液,D不符合题意。故选B。3下列清洗方法中,利用乳化原理的是( )A用自来水洗手B用洗涤剂清洗餐具C用盐酸除水垢D用汽油清洗油污【答案】B【解析】A、用自来水洗手,是用水冲去灰尘等,不符合题意;B、用洗涤剂清洗餐具,是因
4、为洗涤剂中含有乳化剂,具有乳化作用,能将油污乳化为细小油滴,随水冲走,符合题意;C、用盐酸除水垢,是因为盐酸能与碳酸钙,氢氧化镁发生反应,不符合题意;D、用汽油清洗油污,是因为汽油能溶解油污,不符合题意。故选B。4.下列关于溶液的说法中正确的是( )A溶液都是无色透明的混合物B溶液的组成中一定含有水C溶质的溶解度都随温度的升高而增大D溶质以分子或离子的形式均匀分散在溶剂中【答案】D【解析】A、溶液都不一定都是无色透明的混合物,例如硫酸铜溶液是蓝色的;故选项错误;B、溶液的组成中不一定含有水,例如碘酒溶液;故选项错误;C、有些物质的溶解度都随温度的升高而增大,有些物质的溶解度都随温度的升高而减小
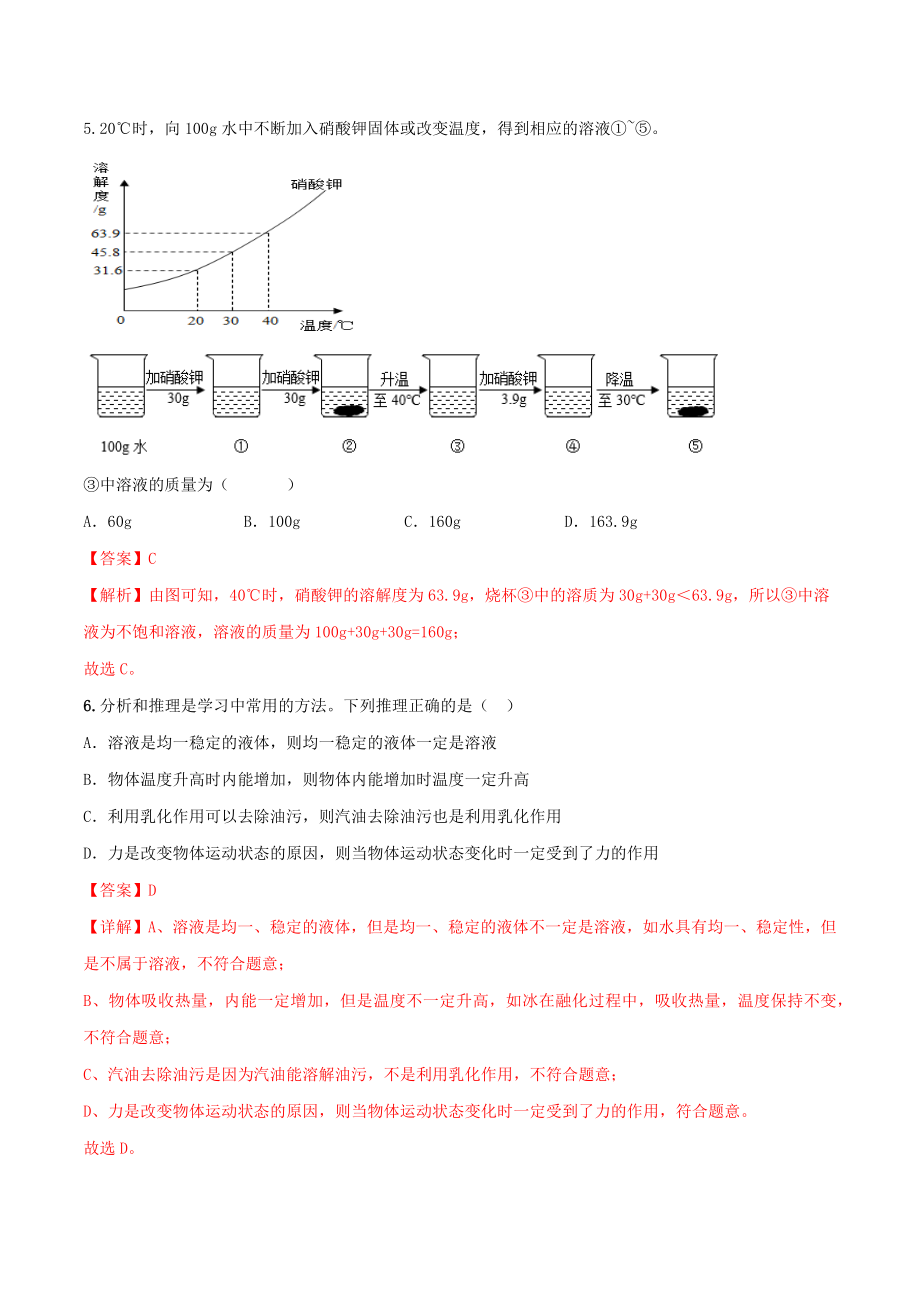
5、;故选项错误;D、溶质以分子或离子的形式均匀分散在溶剂中,符合溶液的均一性,和稳定性;故选项正确;故选:D。5.20时,向100g水中不断加入硝酸钾固体或改变温度,得到相应的溶液。中溶液的质量为( )A60gB100gC160gD163.9g【答案】C【解析】由图可知,40时,硝酸钾的溶解度为63.9g,烧杯中的溶质为30g+30g63.9g,所以中溶液为不饱和溶液,溶液的质量为100g+30g+30g=160g;故选C。6.分析和推理是学习中常用的方法。下列推理正确的是( )A溶液是均一稳定的液体,则均一稳定的液体一定是溶液B物体温度升高时内能增加,则物体内能增加时温度一定升高C利用乳化作用
6、可以去除油污,则汽油去除油污也是利用乳化作用D力是改变物体运动状态的原因,则当物体运动状态变化时一定受到了力的作用【答案】D【详解】A、溶液是均一、稳定的液体,但是均一、稳定的液体不一定是溶液,如水具有均一、稳定性,但是不属于溶液,不符合题意;B、物体吸收热量,内能一定增加,但是温度不一定升高,如冰在融化过程中,吸收热量,温度保持不变,不符合题意;C、汽油去除油污是因为汽油能溶解油污,不是利用乳化作用,不符合题意;D、力是改变物体运动状态的原因,则当物体运动状态变化时一定受到了力的作用,符合题意。故选D。必考点2 饱和溶液与不饱和溶液1.饱和溶液与不饱和溶液的判断:(1)溶解能力:在一定温度下
7、,向某溶液中加入少量的该溶质,观察能否溶解,若能(选填“能”或“不能”)溶解,则溶液达到饱和,否则不饱和。(2).利用溶解度进行判断若 ,溶液为不饱和溶液;若 ,溶液为饱和溶液;若 ,溶液为饱和溶液,且有未溶解固体。 2.饱和溶液与不饱和溶液的转化(1)对于溶解度随温度升高而增大的物质,如NaCl、KNO3。加溶剂、改变温度 蒸发溶剂饱和溶液 不饱和溶液 降温结晶加入溶质、蒸发溶剂、改变温度 结晶(2)对于溶解度随温度升高而减小的物质,如Ca(OH)2。3.结晶(1)定义:溶质从溶液中以晶体的形式析出的过程叫做结晶。(2)方法:蒸发结晶:通过蒸发溶剂的方法使溶质析出,适用于溶解度受温度变化影响
8、较小的物质,如氯化钠。降温结晶(冷却热的饱和溶液):适用于溶解度随温度升高而增大的物质,如硝酸钾。4.易错点a.饱和溶液不一定是浓溶液,如饱和的石灰水溶液就是稀溶液;b.不饱和溶液不一定是稀溶液,如不饱和的氯化钠溶液可能是浓溶液;c.在一定温度时,同一种溶质的饱和溶液要比它的不饱和溶液浓; d.一定条件下,某溶质的饱和溶液对另一种溶质来说,不一定是饱和溶液。如一定温度下氯化钠的饱和溶液中还可以再溶解硫酸铜;e.饱和溶液继续蒸发或一般情况下继续降温会析出晶体,析出晶体后所得的溶液,一定是该温度下该溶质的饱和溶液。f.饱和溶液降低温度不一定会析出晶体,有可能变为不饱和溶液,如Ca(OH)2 的溶液
9、。【考点突破】1.氯化钠和碳酸钠在不同温度时的溶解度如下表,根据此表判断下列说法正确的是( )温度/C10203040溶解度(g/100gH2O)氯化钠35.836.036.336.6碳酸钠12.221.839.753.2A20时,将30g碳酸钠加入100g水中,充分搅拌后得到不饱和溶液B20时,将30g氯化钠加入100g水中,充分搅拌后得到30%的氯化钠溶液C两物质的溶解度相同时的温度范围是在20-30之间D随温度升高氯化钠与碳酸钠溶解度大小的变化趋势相反【答案】C【解析】A、20时,碳酸钠的溶解度为21.8g,20时,将30g碳酸钠加入100g水中,最多只能溶解21.8g,充分搅拌后得到饱
10、和溶液,故选项说法错误;B、20时,氯化钠的溶解度为36.0g,20时,将30g氯化钠加入100g水中,充分搅拌后,得到 100%30%的氯化钠溶液,故选项说法错误;C、由氯化钠和碳酸钠在不同温度时的溶解度表,则两物质的溶解度曲线,在20-30之间出现交叉,故选项说法正确;D、随温度升高氯化钠与碳酸钠溶解度大小的变化趋势相同,故选项说法错误。故选:C2.下图是甲、乙两种物质的溶解度曲线。t3时,将取ag甲和ag乙分别放入100g水中,充分搅拌,然后降温,下列说法不正确的是( )At1时,甲的溶解度小于乙的溶解度B降温至t2时,甲溶液和乙溶液均饱和C降温至t1时,两种溶液中溶质的质量分数相等D若
11、甲中混有少量的乙,可用降温结晶的方法提纯甲【答案】C【解析】A、由溶解度曲线图可知:t1时,甲的溶解度小于乙的溶解度;故选项正确,但不符合题意;B、t2时,甲和乙的溶解度都是ag,升温至t2时,甲溶液和乙溶液均饱和;故选项正确,但不符合题意;C、降温至t1时,甲物质析出固体质量较大,两种溶液中溶质的质量分数:乙甲;故选项错误,但符合题意;D、甲物质的溶解度受温度影响较大,若甲中混有少量的乙,可用降温结晶的方法提纯甲;故选项正确,但不符合题意;故选:C。3.下列说法正确的是( )A人体缺锌会引起生长发育迟缓,因此锌元素摄入的越多越好B用汽油能除去衣服上的油污是乳化现象C两种化合物发生反应生成水,
12、则该反应一定是复分解反应D同一温度下,某固体物质的饱和溶液一定比其不饱和溶液的溶质质量分数大【答案】D【解析】A、各种营养元素的摄入要适量,错误;B、用汽油能除去衣服上的油污是汽油溶解了油污,错误;C、两种化合物发生反应生成水,该反应不一定是复分解反应,例如二氧化碳和氢氧化钙反应生成水,错误;D、同一温度下,某固体物质的饱和溶液一定比其不饱和溶液的溶质质量分数大,正确。故选D。4.饱和溶液和不饱和溶液是可以相互转化的。(1)在一般情况下,将饱和溶液转化为不饱和溶液的方法有_或升高温度;将不饱和溶液转化为饱和溶液的方法有_、蒸发溶剂或降低温度。(2)已知:20时,硝酸钾的溶解度为31.6g;60
13、时,硝酸钾的溶解度为110g20时,向烧杯中加入20mL水(水的密度可近似看做lg/cm3),接下来的实验步骤如下表所示:步骤操作现象分析加入5g硝酸钾,搅拌固体全部溶解步骤_(填序号)形成的溶液是饱和溶液。步骤_(填序号)形成的溶液中溶质的质量分数最大,其质量分数为_(保留至0.1%)再加5g硝酸钾,搅拌_加热至60固体全部溶解再加5g硝酸钾,搅拌_冷却至20_【答案】增加溶剂 增加溶质 有固体剩余 固体全部溶解 固体析出 42.9% 【解析】(1)在一般情况下,将饱和溶液转化为不饱和溶液的方法有增加溶剂或升高温度;将不饱和溶液转化为饱和溶液的方法有增加溶质、蒸发溶剂或降低温度。(2) 20
14、mL水是20g水,因为20时,硝酸钾的溶解度为31.6g,则20g水最多能溶解6.32g硝酸钾, 所以再加5g硝酸钾,搅拌,有固体剩余。60时,硝酸钾的溶解度为110g,则20g水最多能溶解22g硝酸钾,所以第三次加5g硝酸钾,搅拌,固体全部溶解。冷却至20,因为20g水最多能溶解6.32g硝酸钾,所以15g硝酸钾不能全部溶解,会有固体析出。分析:由以上分析可知,步骤形成的溶液是饱和溶液。步骤形成的溶液中溶质的质量分数最大,其质量分数为:=42.9%。必考点3 溶解度和溶解度曲线1.固体溶解度(1)概念:表示在一定温度下,某固态物质在100 g溶剂里达到饱和状态时所溶解的质量。(2)固体溶解度
15、的“四要素”:条件标准状态单位一定温度100克溶剂达到饱和g(3)影响因素:外因:温度。多数固体的溶解度随温度的升高而增大(选填“增大”或“减小”),如硝酸钾、氯化铵等;少数固体的溶解度随温度的升高变化不大,如氯化钠;极少数固体的溶解度随温度升高而减小,如氢氧化钙。内因:溶质、溶剂本身的性质。2.气体溶解度(1)概念:指压强为101 kPa时,在一定温度下,溶解在1体积水里达到饱和状态时的气体体积。(2)影响因素:外因:气体溶解度随着压强的增大而增大,随着温度的降低而增大。内因:溶质、溶剂本身的性质。3. 溶解度曲线(1)意义曲线上的点表示某物质的饱和溶液。曲线的走向表示某物质的溶解度随温度的
16、变化情况。两条溶解度曲线的交点表示两种溶质在某一温度下的溶解度相同。(2)应用判断某种物质的溶解度比较不同物质在同一温度时的溶解度大小(必须指明同一温度,否则无法比较)确定饱和溶液和不饱和溶液的转化方法判断溶液中溶质的质量分数判断物质的溶解度受温度影响变化的趋势判断一定质量饱和溶液中所含溶质的质量判断温度改变时溶液中溶液质量、溶质质量、溶剂质量和溶质质量分数的变化情况,以及物质提纯的方法。(3)判断物质的结晶与提纯方法物质的结晶方法结晶方法 适用范围举例蒸发结晶适用于溶解度随温度变化较小的物质氯化钠冷却热饱和溶液(降温结晶)适用于溶解度随温度变化较大的物质(针对溶解度随温度升高而增大的物质)氢
17、氧化钠 物质的提纯方法结晶常用于分离可溶性固体混合物。a. 当甲中含有少量乙时,可用降温结晶法分离出甲。b. 当乙中含有少量甲时,可用恒温蒸发溶剂法分离出乙。【考点突破】1.水和溶液与我们的生活生产息息相关。下列有关说法中,不正确的是( )A肥皂水可以区分硬水和软水B洗涤剂除去油污的原理是将油污溶解C溶液是均一、稳定的混合物D饱和溶液不一定比不饱和溶液浓度大【答案】B【解析】A、肥皂水可以区分硬水和软水,混合搅拌后,浮渣多,泡沫是的是硬水,反之是软水;故选项正确,但不符合题意;B、洗涤剂除去油污的原理是乳化作用,不是溶解;故选项错误,但符合题意;C、溶液中含有溶质和溶剂,是均一、稳定的混合物;
18、故选项正确,但不符合题意;D、饱和溶液不一定比不饱和溶液浓度大,例如20时,不饱和的硝酸钾(易溶物)溶液质量分数可能大于饱和的氢氧化钙(微溶物)溶液质量分数;故选项正确,但不符合题意;故选:B。2.如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )A使a、c的饱和溶液析出晶体都可以采用降温结晶的方法Bt1时,a、c两种物质的溶液溶质质量分数一定相等Ct2时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是:abcD在t2时,将30ga物质加入50g水中充分溶解,所得溶液质量为80g【答案】C【解析】A、根据图中曲线可知,a的溶解度随温度降低而减小,使其饱和溶液析出晶体可以
19、采用降温结晶的方法。c的溶解度随温度升高而减小,使其饱和溶液析出晶体应采用升温结晶的方法,选项A不正确;B、t1时,a、c两种物质的溶解度曲线相交,溶解度相等,两种物质的饱和溶液溶质质量分数一定相等,否则不一定相等,选项B不正确;C、t2时,a、b、c三种物质的溶解度由大到小的顺序是:abc,溶解度越大,其饱和溶液溶质质量分数越大,因此t2时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是:abc,选项C正确;D、在t2时,a的溶解度是50g,因此将30ga物质加入50g水中充分溶解,只能溶解25g,所得溶液质量为75g,选项D不正确。故选C。3.40 时,向下列3只盛有100 g水


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2023年广东省中考化学一轮复习考点专题1:物质的性质与应用 第6讲溶液含答案 2023 广东省 中考 化学 一轮 复习 考点 专题 物质 性质 应用 溶液 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-234228.html