 2018年中考化学真题分类汇编解析:工艺流程1
2018年中考化学真题分类汇编解析:工艺流程1
《2018年中考化学真题分类汇编解析:工艺流程1》由会员分享,可在线阅读,更多相关《2018年中考化学真题分类汇编解析:工艺流程1(18页珍藏版)》请在七七文库上搜索。
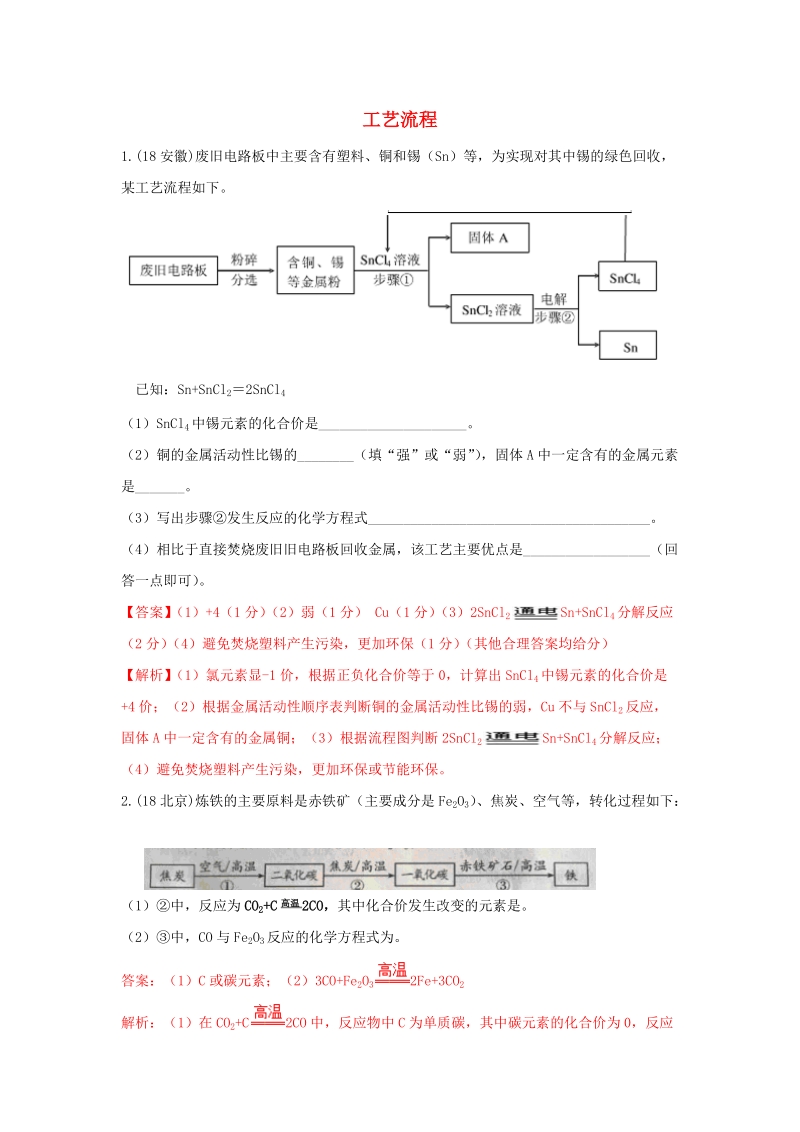
1、工艺流程1.(18 安徽)废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl 22SnCl 4(1)SnCl 4中锡元素的化合价是_。(2)铜的金属活动性比锡的_(填“强”或“弱” ) ,固体 A 中一定含有的金属元素是_。(3)写出步骤发生反应的化学方程式_。(4)相比于直接焚烧废旧旧电路板回收金属,该工艺主要优点是_(回答一点即可) 。【答案】 (1)+4(1 分) (2)弱(1 分) Cu(1 分) (3)2SnCl 2 Sn+SnCl4分解反应(2 分) (4)避免焚烧塑料产生污染,更加环保(1 分) (其他合理答案均给分)【解析
2、】 (1)氯元素显-1 价,根据正负化合价等于 0,计算出 SnCl4中锡元素的化合价是+4 价;(2)根据金属活动性顺序表判断铜的金属活动性比锡的弱,Cu 不与 SnCl2反应,固体 A 中一定含有的金属铜;(3)根据流程图判断 2SnCl2 Sn+SnCl4分解反应;(4)避免焚烧塑料产生污染,更加环保或节能环保。2.(18 北京)炼铁的主要原料是赤铁矿(主要成分是 Fe2O3) 、焦炭、空气等,转化过程如下:(1)中,反应为 CO2+C 高温 2CO,其中化合价发生改变的元素是。(2)中,CO 与 Fe2O3反应的化学方程式为。答案:(1)C 或碳元素;(2)3CO+Fe 2O3 2Fe
3、+3CO2解析:(1)在 CO2+C 2CO 中,反应物中 C 为单质碳,其中碳元素的化合价为 0,反应后只有一种生成物,CO 中的碳元素化合价为+2 价,故化合价发生改变的元素是碳元素;(2)中的反应为一氧化碳在高温的条件下还原氧化铁,其方程式为:3CO+Fe2O3 2Fe+3CO2。3、(18 北京)为保护绿水青山,可将工业残留的钡渣(主要成分为碳酸钡(BaCO 3) )进行无害化处理,制取化工原料;硫酸钡(BaSO 4) 。主要流程如下:已知:BaSO 4难溶于水,氯化钡(BaCl 2)可溶于水。(1)粉碎钡渣的目的是。(2)反应釜 1 中的气体 X 为。(3)放反应釜 2 中发生复分解
4、反应的化学方程式为。【答案】 (1)增大反应物的接触面积,加快反应速率,使其充分反应(答案合理即可)(2)CO 2;(3)BaCl 2+H2SO4=BaSO4+2HCl【解析】 (1) “粉碎” 、 “破碎” 、 “研磨”固体,其作用大多是增大反应物的接触面积,加快反应速率,使其充分反应;(2)钡渣的主要成分是碳酸钡(BaCO 3) ,加入盐酸后其反应的方程式为:BaCO3+2HCl=BaCl2+H2O+CO2,反应釜 1 中的气体 X 为 CO2;(3)放反应釜 2 中发生的反应为氯化钡溶液与硫酸反应,其反应方程式为:BaCl2+H2SO4=BaSO4+2HCl4.(18 福建)以某矿山酸性
5、废水(主要含硫酸、硫酸铁、硫酸铜和硫酸锌等)为原料,通过下述流程可将废水中的铁、铜和锌分步沉淀,实现回收利用。(1)步骤中,加入 Ca(OH)2有两个作用。一是中和废水中的硫酸,该反应的化学方程式为_;二是将硫酸铁转化为 Fe(OH)3,该反应属于_(填基本反应类型)。(2)步骤中,锌泥中最主要的含锌化合物的化学式为_;(3)为分步回收铁、铜、锌等金属资源且直接得到铜单质,只需改变上述流程中的某步骤加入的试剂即可。该步骤和应加入的试剂分别是_。【答案】(1).Ca(OH) 2+H2SO4=CaSO4+2H2O(2).复分解反应(3).Zn(OH) 2(4).步骤锌【解析】(1)根据氢氧化钙与硫
6、酸反应生成硫酸钙和水解析;根据两种化合物互相交换成分,生成另外两种化合物且生成物中有气体、沉淀或水生成解析;(2)根据硫酸锌与氢氧化钙反应生成氢氧化锌解析;(3)根据锌能置换出硫酸铜溶液中的铜解析。(1)氢氧化钙与硫酸反应生成硫酸钙和水,反应的化学方程式为 Ca(OH)2+H2SO4=CaSO4+2H2O;由反应的化学方程式3Ca(OH)2+Fe2(SO4)3=3CaSO4+2Fe(OH)3可知,该反应属于复分解反应;(2)硫酸锌与氢氧化钙反应生成氢氧化锌,故锌泥中最主要的含锌化合物的化学式为 Zn(OH)2;(3)锌能置换出硫酸铜溶液中的铜,故在步骤中加入锌即可。5.(18 广州)氧化锌(Z
7、nO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下(1)推测草酸的化学式是;(2)“沉锌”过程中发生复分解反应,反应的化学方程式是(3) “操作 A”的名称是 实验室常用的研磨仪器是;(4)“高温灼烧”时草酸锌分解,反应的化学方程式是。【答案】 (1)H 2C2O4( 2) (NH4)2C2O4+ZnCl2=ZnC2O4+2NH4Cl( 3) 过滤;研钵和研杵( 4) ZnC2O4高温ZnO+CO+CO 2【解析】 (1)由草酸铵化学式可以得知草酸根的书写方式以及化合价,然后即可推出草酸的化学式;(2)已知该反应为复分解反应,且在流程中可以得知草酸锌为沉淀,反应物为草酸铵和锌与盐酸反应
8、的产物,故可以书写方程式;(3)操作A分开了溶液和沉淀草酸锌,故为过滤;实验室常用研磨仪器为研钵和研杵。(4)已知该反应为分解反应,条件为高温,且生成混合气体,即一种以上气体,故分析及配平可以得知为一氧化碳和二氧化碳。6.(18 广东)孔雀石主要成分为 Cu2(OH)2CO3(难溶于水),还含有少量 SiO2(难溶于水、不与稀硫酸反应)、Fe 2O3等杂质。现以孔雀石为原料制取胆矾(CuSO 45H2O)的部分工艺流程如图。请回答:(1)滤渣 b 的化学式为_。(2)溶液 c 中的溶质有(写化学式):H 2SO4、_、_。(3)盐溶液 d 的颜色为_;实验室蒸发溶液时用到的玻璃仪器有_(写 1
9、 种)。(4)在气体 a 生成 CaCO3的过程中,发生反应:CO 2+CaCl2+2NH3+H2O=CaCO3+2X,X 的名称为_;孔雀石与稀硫酸反应生成气体 a 的化学方程式为_。【答案】(1).SiO 2(2).CuSO4(3).Fe2(SO 4) 3(4).蓝色(5).玻璃棒(6).氯化铵(7).Cu 2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2【解析】(1)根据二氧化硅难溶于水、不与稀硫酸反应解析;(2)根据碱式碳酸铜与稀硫酸反应生成硫酸铜,氧化铁与稀硫酸反应生成硫酸铁解析;(3)根据结晶后得到 CuSO45H2O可知,盐溶液 d 是硫酸铜溶液解析;根据实验室蒸
10、发溶液时用玻璃棒进行搅拌解析;(4)根据质量守恒定律分析解析;根据碱式碳酸铜与稀硫酸反应生成硫酸铜、水和二氧化碳解析。(1)二氧化硅难溶于水、不与稀硫酸反应,故滤渣 b 为二氧化硅,化学式 SiO2;(2)Cu 2(OH)2CO3与稀硫酸反应生成硫酸铜,氧化铁与稀硫酸反应生成硫酸铁。故溶液 c 中的溶质有H2SO4、CuSO 4、Fe 2(SO 4) 3;(3)盐溶液 d 为硫酸铜溶液,颜色为蓝色;实验室蒸发溶液时用到的玻璃仪器有玻璃棒;(4)反应前后 C、O、Ca、Cl、N、H 的原子个数分别为1、3、1、2、2、8,1、3、1、0、0、0。反应前后 Cl、N、H 原子个数相差 2、2、8。
11、又 X前的化学计量数为 2,故 1 个 X 分子中含有 Cl、N、H 原子个数为 1、1、4,故 X 的化学式为 NH4Cl,名称为氯化铵;碱式碳酸铜与稀硫酸反应生成硫酸铜、水和二氧化碳,反应的化学方程式为 Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2。7.(18 梧州)工业上为提高煤的综合利用,可采用用下列流程;(1)在加压条件下,把二氧化碳通入溶有氨气的饱和食盐水中,最终可制得一种含氯元素的氮肥(填化学式)和一种水溶液显碱性的盐(填化学式) 。(2)写出流程中 CO 与 H2转化为 C8H16的化学方程式【答案】 (1)NH 4ClNaHCO3;(2)8CO+16H
12、 2一 定 条 件C8H16+8H2O。【解析】 (1)根据质量守恒定律判断可制得一种含氯元素的氮肥 NH4Cl 和 NaHCO3;(2)根据流程图判断:8CO+16H 2一 定 条 件C8H16+8H2O。8.(18 咸宁)某种手机电路板中含有 Fe、Cu、Au、Ag、Ni(镍,银白色金属)等金属,如图是某工厂回收部分金属的流程图。已知:2Cu+O 2+2H2SO4 2CuSO4+2H2O(1)操作的名称是过滤。(2)写出滤液中金属阳离子符号 Fe2+。(3)写出滤液和铁粉发生反应的一个化学方程式 Fe+CuSO4=FeSO4+Cu。(4)Cu、Ag、Ni 在溶液中的活动性由强到弱的顺序依次
13、是 Ni、Cu、Ag。【答案】:(1)过滤;(2)Fe 2+;(3)Fe+CuSO 4=FeSO4+Cu;(4)Ni、Cu、Ag。【解析】解:排在氢前面的金属可以将酸中的氢置换出来,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,所以(1)操作可以将不溶性固体从溶液中分离出来,所以操作的名称是过滤;(2)铁在置换反应中生成亚铁离子,所以滤液中金属阳离子符号 Fe2+;(3)滤液和铁粉发生的反应是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;(4)镍会与硫酸反应生成滤液中的一种成分,铜可以将银置换出来,所以 Cu、Ag、Ni在溶液中的活动性由强到弱的顺
14、序依次是:Ni、Cu、Ag。9.(18 娄底)2018 年 5 月 23 日至 25 日,第九届中国卫星导航年会在哈尔滨拉开帷幕,中海达、华大北斗等一批国内企业先后发布了自主研发的北斗芯片产品。芯片的主要成分是硅,如图是工业上以石英砂(SiO 2)为主要原料制取纯硅的种方法,请回答以下问题。(1)地壳中硅元素的含量仅次于氧元素;(2)写出反应的化学方程 SiO2+2C Si+2CO;(3)反应的基本反应类型是置换反应;(4)尾气氯化氢必须收集处理,不能排放到空气中,请简要说明原因氯化氢会污染环境。【答案】氧;SiO 2+2C Si+2CO;置换反应;氯化氢会污染环境。【解析】解:(1)地壳中元
15、素含量前五位是氧、硅、铝、铁和钙,故地壳中硅元素的含量仅次于氧元素;(2)反应是二氧化硅和碳在高温下反应生成硅和一氧化碳,该反应的化学方程为 SiO2+2C Si+2CO;(3)反应是四氯化硅与氢气高温反应生成硅和氯化氢,的基本反应类型是置换反应;(4)尾气氯化氢必须收集处理,不能排放到空气中,请简要说明原因氯化氢会污染环境。10.(18 长沙)我市教育主管部门为了让同学们过好传统佳节一一端午节,特意将中考提前一天。化学兴趣小组的同学们为庆祝端午佳节,决定自己动手制作传统食品一一皮蛋.制作皮蛋料泥的原料主要有:生石灰、纯碱、草木灰(含 K2CO3)等.将他们按一定比例混合加入适量水得到皮蛋料泥
16、.料泥的主要成分是什么呢?同学们进行了如图所示的探究:(1)步骤的操作所需的玻璃仪器有:烧杯、玻璃棒、_;(2)步骤的现象说明滤渣中一定含有的物质为:_;(3)由上述实验现象推断,滤液中的溶质一定含有:_;【答案】(1).漏斗(2).碳酸钙(或 CaCO3)(3).NaOH、Ca(OH) 2、KOH(或氢氧化钠、氢氧化钙、氢氧化钾)【解析】本题考查了实验探究物质的组成成分;过滤所用的仪器,生石灰的性质,碳酸盐的检验等。根据问题情景,找到实验的反应原理;再根据实验的反应原理,分析推断出该物质的组成成分。(1)步骤的主要操作是过滤,过滤所需的玻璃仪器有:烧杯、玻璃棒、漏斗;(2)原料中的生石灰与水
17、反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾。步骤滴加盐酸观察到有气泡产生,滤渣中含碳酸盐,可判断滤渣中一定含有物质是碳酸钙(或 CaCO3) ;(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾。步骤向滤液中加入酚酞,溶液变红色,说明滤液中存在氢氧根离子;步骤向滤液中滴加盐酸无气体产生,说明滤液中没有碳酸盐;步骤向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,滤液中的溶质一定含有NaOH、Ca(OH) 2、KOH(或氢氧化钠、氢氧化钙、氢氧化钾) 。11.(18 连云港)过氧化钙(Ca
18、O 2)是用途广泛的优良供氧剂。以电石渣主要成分为 Ca(OH)2,含少量 CaCO3为原料制备 CaO2的一种工艺流程如下:【查阅资料】I.Ca(OH) 2+2NH4Cl=CaCl2+2NH3H2O.CaCl 2+2NH3H2O+H2O2+6H2O=CaO28H2O+2NH 4Cl.CaO 28H2O 在水中不太稳定,会缓慢分解。(1)“提取 Ca(OH)2”时反应的基本类型是_;Ca(OH) 2的俗名为_;“过滤 1”所得滤渣的主要成分是_。(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边缘略低于漏斗口、_。生产过程中为了精确测定溶液的 pH,常使用
19、_(填仪器名称)。(3)在其他条件不变的情况下,制备 CaO28H2O 的反应时间(t)对其产率(w)的影响如图所示。平均反应速率最快的时间段为:_(填字母)。a. 010min b. 1020minc. 2030min d.3040min30min 后,w 开始下降的主要原因是_。(4)为了测定加入的 NH4Cl 溶液中溶质的质量分数,取 30.00gNH4Cl 溶液于烧杯中,加入稍过量的 AgNO3溶液,完全反应后过滤、洗涤、干燥、称量,得到 14.35g 白色固体。通过计算确定该溶液中 NH4Cl 的质量分数(精确到 0.1%)_。【答案】(10 分)(1)复分解反应熟石灰(或消石灰)C
20、aCO 3(碳酸钙)(3 分)(2)液面低于滤纸边缘 pH 计(酸度计或 pH 测定仪)(2 分)(3)aCuO 28H2O 在水中不太稳定会缓慢分解(2 分)(4)17.8%(1 分)【解析】(1)提取 Ca(OH)2的化学方程式:Ca(OH) 2+2NH4Cl=CaCl2+2NH3H2O,属于复分解反应;Ca(OH) 2的俗名为熟石灰(或消石灰);CaCO 3(碳酸钙)难溶于水,是滤渣的主要成分;(2)过滤操作时,要遵循“一贴、二低、三靠”原则。 “一贴”是指滤纸紧贴漏斗内壁;“二低”是指滤纸边缘低于漏斗边缘,滤液液面低于滤纸边缘;“三靠”玻璃棒紧靠滤纸三折处,滤液烧杯紧靠玻璃棒,漏斗器下
21、端紧靠烧杯内壁;pH 计(酸度计或 pH 测定仪)可以精确测定溶液的 pH;(3)据图判断 010min,平均反应速率最快;CuO 28H2O 在水中不太稳定会缓慢分解,使反应减慢;(4)设 30.00gNH4Cl 溶液中含 NH4Cl 的质量为 x。NH4Cl+AgNO3=AgCl+NH 4NO353.5143.5x14.35g53.5/x=143.5/14.35gx=5.35g所以该溶液中 NH4Cl 的质量分数:(5.35g/30.0g)100%17.8%。12.(18 宿迁)海洋是人类巨大的资源宝库,下图为从海水中提取金属镁的简易流程图。(1)海洋中含量最多的物质是_;(2)实验室中进


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2018 年中 化学 分类 汇编 解析 工艺流程
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
文档标签
- 工艺流程
- 焊工工艺习题册的答案
- CASS工艺处理污水
- 装配工艺规范标准
- 2018年中考化学真题分类汇编解析溶液
- 2018年中考化学真题分类汇编解析盐化肥
- 2018年中考化学真题分类汇编考点34工艺流程含答案
- 2018年中考化学真题分类汇编解析化学用语
- 2018年中考化学真题分类汇编解析常见气体的制取
- 2018年中考化学真题分类汇编解析工艺流程1
- 2018年中考化学真题分类汇编解析工艺流程2
- 2018年中考化学真题分类汇编解析科学探究
- 2018年中考化学真题分类汇编解析创新题
- 2018年中考化学真题分类汇编解析化学与环境一
- 2018年中考化学真题分类汇编解析化学与生活
- 2018年中考化学真题分类汇编解析物质的推断1
- 高中工艺流程
- 中考化学流程
- 中考化学工艺流程
- 化学流程



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-58941.html