 吉林省2019届高三第一次联合模拟考试化学试卷(含答案)
吉林省2019届高三第一次联合模拟考试化学试卷(含答案)
《吉林省2019届高三第一次联合模拟考试化学试卷(含答案)》由会员分享,可在线阅读,更多相关《吉林省2019届高三第一次联合模拟考试化学试卷(含答案)(9页珍藏版)》请在七七文库上搜索。
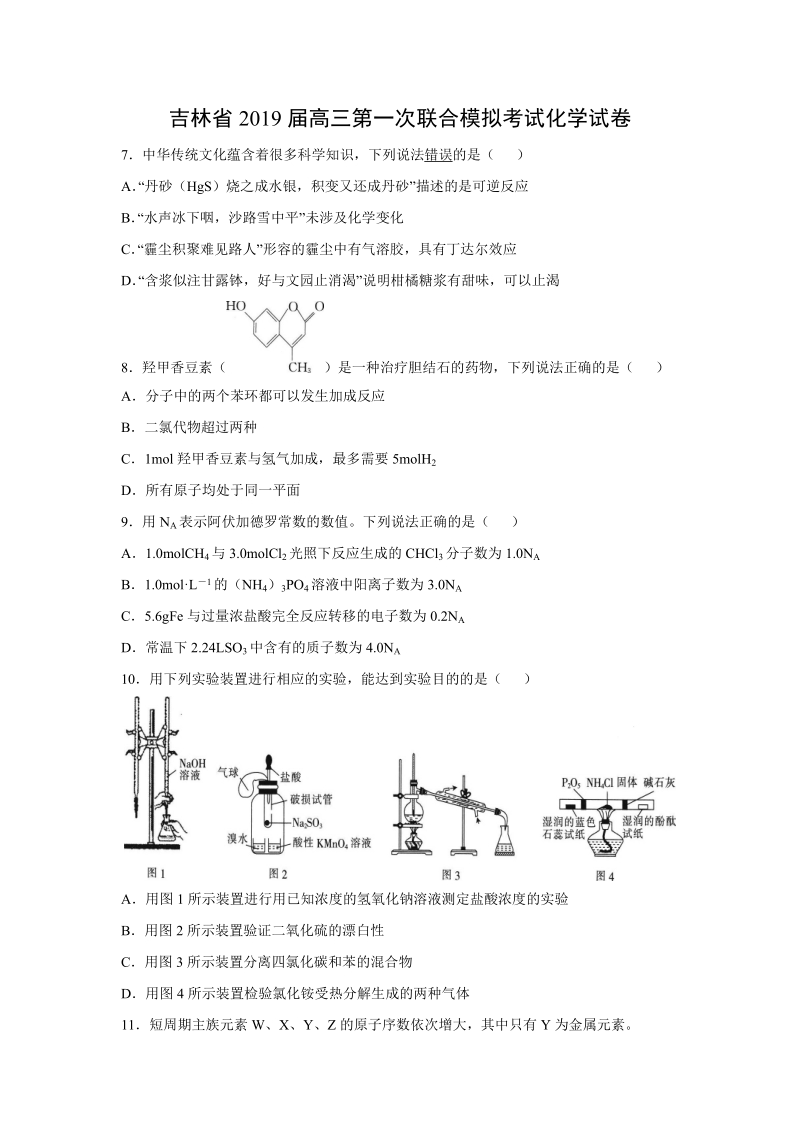
1、吉林省 2019 届高三第一次联合模拟考试化学试卷7中华传统文化蕴含着很多科学知识,下列说法错误的是( )A “丹砂(HgS)烧之成水银,积变又还成丹砂 ”描述的是可逆反应B “水声冰下咽,沙路雪中平”未涉及化学变化C “霾尘积聚难见路人”形容的霾尘中有气溶胶,具有丁达尔效应D “含浆似注甘露钵,好与文园止消渴”说明柑橘糖浆有甜味,可以止渴8羟甲香豆素( )是一种治疗胆结石的药物,下列说法正确的是( )A分子中的两个苯环都可以发生加成反应B二氯代物超过两种C1mol 羟甲香豆素与氢气加成,最多需要 5molH2D所有原子均处于同一平面9用 NA 表示阿伏加德罗常数的数值。下列说法正确的是( )
2、A1.0molCH 4 与 3.0molCl2 光照下反应生成的 CHCl3 分子数为 1.0NAB1.0molL 1 的(NH 4) 3PO4 溶液中阳离子数为 3.0NAC5.6gFe 与过量浓盐酸完全反应转移的电子数为 0.2NAD常温下 2.24LSO3 中含有的质子数为 4.0NA10用下列实验装置进行相应的实验,能达到实验目的的是( )A用图 1 所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验B用图 2 所示装置验证二氧化硫的漂白性C用图 3 所示装置分离四氯化碳和苯的混合物D用图 4 所示装置检验氯化铵受热分解生成的两种气体11短周期主族元素 W、X 、Y 、Z 的原子序
3、数依次增大,其中只有 Y 为金属元素。W、Y、Z 最外层电子数之和为 12;W 与 X、Y 与 Z 分别同周期;X 与 Z 形成的化合物可被氢氟酸腐蚀。下列说法错误的是( )A常温常压下 W 的单质为气态BZ 的氢化物为共价化合物CX 和 Y 的原子半径大小:X YDX 与 Z 形成的化合物属于碱性氧化物12铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为,电池结构如图所示。下列说法正确的是( 6 6AlLi(PF)AlCLiPFxx放 电充 电)A放电时,外电路中电子向铝锂电极移动B充电时,应将铝石墨电极与电源负极相连C放电时,正极反应式为 66C(PF)ePFxxD充电时,若电路
4、中转移 1mol 电子,则阴极质量增加 9g13下图为常温下向 10mL0.1molL1 NH3H2O 中加入等浓度的盐酸时 NH3H2O 的物质的量随 V(盐酸)的变化曲线, (电离度为已电离的 NH3H2O 占初始时 NH3H2O 的百分比)下列说法正确的是( )A测得 a 点时溶液的 pH11 ,则 NH3H2O 的电离度为 1Bb 点时溶液的 pH7C水的电离程度:bcDc 点时溶液中存在关系式: 4322(Cl)(NH)(O)cc26一种以软锰矿(主要成分为 MnO2、SiO 2、Al 2O3)和黄铁矿( FeS2、SiO 2)为原料冶炼金属锰的工艺流程如图所示:已知相关金属离子c(
5、M n )0.1molL 1 形成氢氧化物沉淀的 pH 如下:金属离子 Fe3 Mn2 Al3开始沉淀的 pH 2.7 8.3 3.2沉淀完全的 pH 3.7 9.8 5.0回答下列问题:(1)MnO 2 本身不能溶于硫酸,但是在 Fe2 的作用下却能溶解,写出该反应的离子方程式:_。(2)滤渣 1 的成分除了 SiO2 外,还有一种淡黄色的物质是_(填化学式) 。(3)除杂步骤中加入的 MnCO3 的作用是_,该过程需调节溶液 pH 的范围是_ ,若把 pH 调得过高,其后果是_。(4)用惰性电极进行电解,电解刚开始时阴极的电极反应式为_,电解后阳极的电解质溶液可返回_(填“酸浸”“ 除杂”
6、或“电解”)工序继续使用。27世界能源消费的 90以上依靠化学技术。回答下列问题:(1)质子交换膜燃料电池中作为燃料的 H2 通常来自水煤气。已知: H1110.35kJmol 121C(s)O(g)()2H2(g)O 2(g)2H 2O(l ) H2571.6kJmol 1H2O(l)H 2O(g) H344.0kJmol 1则反应 C(s ) H2O(g) CO(g)H 2(g) H4_。某实验小组在实验室模拟反应 C(s)H 2O(g) CO(g)H 2(g) ,其平衡常数表达式为K_。一定温度下,在 2L 盛有足量炭粉的恒容密闭容器中通入 0.8molH2O,6min时生成 0.7gH


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 吉林省 2019 届高三 第一次 联合 模拟考试 化学 试卷 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-58973.html